Vacunas anticovid de ARN para pequeños de 6 meses a 5 años
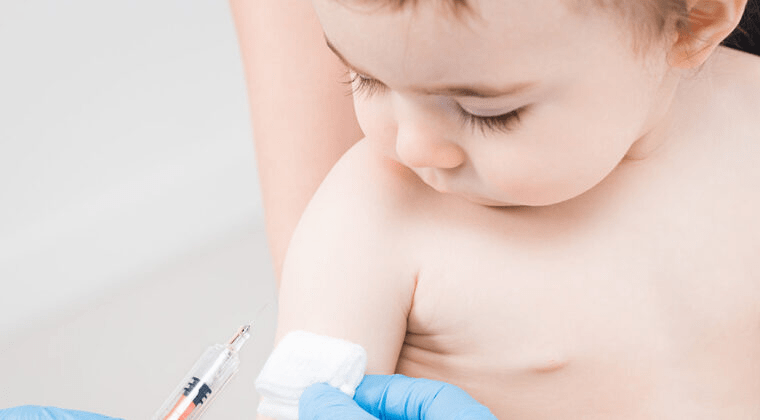
La población mundial, en general, tiene a su disposición diferentes plataformas de vacunas contra la COVID-19, incluyendo dosis de refuerzo, las cuales ayudan principalmente a que uno, si contrae la enfermedad del coronavirus, no resulte en un cuadro grave. Ese es el objetivo principal de las diferentes vacunas contra la COVID-19.

A medida que demostraban efectividad y seguridad, vacunas de diferentes plataformas fueron aprobadas para mayores de 18 años; en tanto, el grupo de niños y adolescentes requería un estudio diferente.

Por fortuna, niños y adolescentes de entre 5 a 17 años pudieron acceder a las vacunas este año (en este caso con la vacuna de Pfizer y, en algunos países, las vacunas de virus inactivado). Sin embargo, todavía faltaba un grupo de personitas quienes suelen estar más expuestas al virus debido a que no pueden usar tapabocas: los bebés de 6 meses a 4 años.
Luego de una serie de análisis clínicos y evaluaciones de dosis, Pfizer y Moderna recibieron la aprobación de la FDA pare el uso de sus vacunas en niños de 6 meses a 4 y 5 años. En el caso de la vacuna de Moderna, también presentaron los documentos referentes a la vacuna para personas hasta los 17 años. La vacuna COVID de Moderna estaba aprobada solo en adultos mayores de 18 años.
Las vacunas anti-COVID-19 de Moderna y Pfizer/BioNTech demostraron ser seguras y efectivas para niños menores de 5 años, haciendo posible planificación para la inmunización del único grupo de edad que aún espera acceso.
Moderna propone un esquema de dos dosis para su vacuna anti-COVID-19. Las dosis varían de acuerdo a grupos de edades: de 12 a 17 años (100 μg), de 6 a 11 años (50 μg) y de 6 meses a 5 años (25 μg).
El resultado de los ensayos clínicos mostró que la eficacia de la vacuna de Moderna fue del 36,8 % para las edades de 2 a 5 años y del 50,6 % para las edades de 6 a 23 meses, durante un período de evaluación en el cual predominaba la variante Ómicron, según el documento informativo. El Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) analizó si un régimen de dos dosis de la vacuna de mRNA de Moderna es seguro y eficaz para prevenir la COVID-19 en niños de 6 meses a 17 años.
Para la vacuna de Moderna, entre los participantes de 12 a 17 años, la eficacia de la vacuna fue del 93,3 % durante un período en el que predominaban las variantes ancestrales y Alfa. La eficacia de la vacuna fue del 76,8 % en las edades de 6 a 11 años, durante un período en el que Delta era la variante más prevalente. En general, los niños más pequeños (de 6 meses a 11 años) experimentaron menos eventos adversos que los adolescentes, con la excepción de las fiebres, anotó el documento informativo de la FDA.
Las principales reacciones adversas en el grupo de 6 a 23 meses fueron sensibilidad en el lugar de la inyección, irritabilidad, somnolencia, disminución del apetito y fiebre. Las tasas de reacciones adversas para esas personas fueron más bajas que las del grupo de edad de 5 a 11 años
En el caso de la vacuna de Pfizer, el Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) evaluó el siguiente esquema: tres dosis de 3 µg de ARNm por dosis, administradas con 3 semanas de diferencia. Según los informes presentados, la vacuna de Pfizer cumplió con los criterios de éxito en las edades de 6 a 23 meses, y en las edades de 2 a 4 años. Los datos mostraron que la vacuna era segura y eficaz en estos grupos de edad. La eficacia de la vacuna de Pfizer fue del 80,4% en general para el grupo completo estudiado, en el grupo de 6 a 23 meses fue de 75,6%; y, en el grupo de 2 a 4 años, de 82,4%.
Estados Unidos y otros países, ya han ordenado vacunas para el rango de edad de 6 meses a 4 años, de manera a comenzar la inmunización lo antes posible.




